Mục lục bài viết
- 1 1. Tổng quan về Axit Clohydric (HCl)
- 2 2. Nguyên lý sản xuất HCl trong công nghiệp
- 3 3. Sơ đồ quy trình sản xuất HCl
- 4
- 5 4. Giai đoạn 1: Tổng hợp khí HCl (Tháp T1)
- 6 5. Giai đoạn 2: Hấp thụ khí HCl tạo dung dịch
- 7 6. Tháp hấp thụ sơ cấp (T2)
- 8 7. Tháp hấp thụ hoàn thiện (T3)
- 9 8. Thu hồi dung dịch HCl
- 10 9. Các yếu tố ảnh hưởng đến hiệu suất sản xuất
- 11 10. Ưu điểm của phương pháp tổng hợp HCl
- 12 11. Nhược điểm và rủi ro
- 13 12. Ứng dụng của HCl sản xuất công nghiệp
- 14 13. Tiêu chuẩn chất lượng HCl
- 15 14. An toàn trong sản xuất và sử dụng
- 16 15. Xu hướng công nghệ sản xuất HCl hiện đại
- 17 16. Kết luận
- 18 17. Liên hệ tư vấn và cung cấp HCl
1. Tổng quan về Axit Clohydric (HCl)
Axit Clohydric (Hydrochloric Acid) là một trong những hóa chất vô cơ quan trọng bậc nhất trong công nghiệp hiện đại. Công thức hóa học là HCl, tồn tại dưới dạng khí không màu (khí HCl) hoặc dung dịch trong nước (axit HCl).
Thông tin kỹ thuật cơ bản:
- Tên hóa học: Axit Clohydric
- Công thức: HCl
- CAS: 7647-01-0
- HS Code: 2806.10.00
- Tính chất: Axit mạnh, ăn mòn cao, tan hoàn toàn trong nước
HCl được sử dụng rộng rãi trong:
- Xử lý kim loại (tẩy gỉ thép)
- Sản xuất hóa chất (PVC, Clorua)
- Xử lý nước
- Công nghiệp thực phẩm, dược phẩm
Để đáp ứng nhu cầu lớn, HCl được sản xuất chủ yếu bằng phương pháp tổng hợp từ khí Hydro (H₂) và Clo (Cl₂), sau đó hấp thụ vào nước.
2. Nguyên lý sản xuất HCl trong công nghiệp
Phản ứng cốt lõi tạo ra HCl:
H2 + Cl2 → 2HCl + Q
Đây là phản ứng:
- Tỏa nhiệt mạnh (phản ứng cháy)
- Diễn ra nhanh khi có nguồn kích hoạt (tia lửa hoặc nhiệt)
Khí HCl sinh ra sẽ được dẫn vào hệ thống hấp thụ để tạo dung dịch axit.
3. Sơ đồ quy trình sản xuất HCl
Quy trình sản xuất HCl công nghiệp gồm 2 giai đoạn chính:
- Tổng hợp khí HCl
- Hấp thụ tạo dung dịch HCl
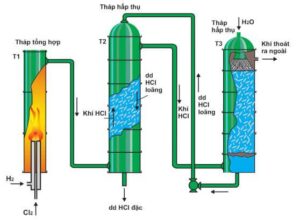
Hình bạn cung cấp mô tả hệ thống gồm:
- Tháp tổng hợp (T1)
- Tháp hấp thụ trung gian (T2)
- Tháp hấp thụ hoàn thiện (T3)
4. Giai đoạn 1: Tổng hợp khí HCl (Tháp T1)
4.1 Nguyên liệu đầu vào
- Khí Hydro (H₂)
- Khí Clo (Cl₂)
Hai khí này thường được lấy từ:
- Điện phân dung dịch NaCl
- Công nghiệp hóa chất Clo – kiềm
4.2 Cơ chế phản ứng
Trong tháp T1:
- H₂ và Cl₂ được đưa vào buồng đốt
- Phản ứng xảy ra dưới điều kiện nhiệt độ cao
- Ngọn lửa cháy tạo ra khí HCl
Đặc điểm kỹ thuật:
- Nhiệt độ rất cao
- Phản ứng tỏa nhiệt mạnh
- Phải kiểm soát tỷ lệ khí để tránh nổ
4.3 Yêu cầu kỹ thuật
- Tỷ lệ H₂ : Cl₂ phải chính xác
- Hệ thống chống cháy nổ
- Vật liệu chịu ăn mòn cao (thường là thép đặc biệt hoặc lót gạch chịu acid)
Khí HCl sinh ra sẽ được dẫn sang tháp hấp thụ.
5. Giai đoạn 2: Hấp thụ khí HCl tạo dung dịch
5.1 Nguyên lý hấp thụ
Khí HCl tan rất mạnh trong nước:
HCl(khí) + H2O → HCl(dd)
Quá trình hấp thụ cần:
- Tăng diện tích tiếp xúc khí – lỏng
- Kiểm soát nhiệt độ (vì hòa tan tỏa nhiệt)
6. Tháp hấp thụ sơ cấp (T2)
6.1 Chức năng
- Hấp thụ phần lớn khí HCl
- Tạo dung dịch HCl nồng độ trung bình
6.2 Cấu tạo
- Tháp dạng đứng
- Bên trong có đệm (packing) để tăng diện tích tiếp xúc
- Nước hoặc dung dịch tuần hoàn chảy từ trên xuống
- Khí HCl đi từ dưới lên
6.3 Quá trình vận hành
- Khí HCl tiếp xúc với nước
- HCl hòa tan nhanh
- Tạo dung dịch HCl loãng → đậm dần
6.4 Sản phẩm
- Dung dịch HCl nồng độ khoảng 20–30%
Phần khí chưa hấp thụ hết sẽ tiếp tục sang tháp T3.
7. Tháp hấp thụ hoàn thiện (T3)
7.1 Mục đích
- Hấp thụ triệt để khí HCl còn lại
- Giảm khí thải ra môi trường
7.2 Đặc điểm vận hành
- Sử dụng nước sạch từ trên xuống
- Khí đi ngược dòng
- Hiệu suất hấp thụ rất cao
7.3 Kiểm soát môi trường
- Khí thoát ra gần như không còn HCl
- Đáp ứng tiêu chuẩn khí thải công nghiệp
8. Thu hồi dung dịch HCl
Dung dịch HCl sau khi hấp thụ được:
- Thu ở đáy tháp
- Điều chỉnh nồng độ
Các mức phổ biến:
- HCl 32%
- HCl 35%
- HCl kỹ thuật hoặc tinh khiết
9. Các yếu tố ảnh hưởng đến hiệu suất sản xuất
9.1 Nhiệt độ
- Nhiệt độ cao làm giảm khả năng hòa tan
- Cần hệ thống làm mát
9.2 Áp suất
- Áp suất cao giúp tăng hấp thụ
- Nhưng cần thiết kế an toàn
9.3 Thiết kế tháp
- Loại đệm (packing)
- Chiều cao tháp
- Tốc độ dòng
9.4 Độ tinh khiết nguyên liệu
- H₂ và Cl₂ phải sạch
- Tránh tạp chất gây ăn mòn hoặc phản ứng phụ
10. Ưu điểm của phương pháp tổng hợp HCl
- Hiệu suất cao (gần 100%)
- Nguyên liệu sẵn có
- Chi phí sản xuất thấp
- Dễ mở rộng quy mô
- Kiểm soát chất lượng tốt
11. Nhược điểm và rủi ro
- Nguy cơ cháy nổ (H₂ + Cl₂)
- Ăn mòn thiết bị mạnh
- Yêu cầu hệ thống an toàn cao
- Phải xử lý khí thải nghiêm ngặt
12. Ứng dụng của HCl sản xuất công nghiệp
12.1 Ngành kim loại
- Tẩy rỉ thép
- Làm sạch bề mặt kim loại
12.2 Ngành hóa chất
- Sản xuất PVC
- Tổng hợp muối clorua
12.3 Xử lý nước
- Điều chỉnh pH
- Trung hòa kiềm
12.4 Công nghiệp thực phẩm
- Điều chỉnh độ axit
- Chế biến phụ gia
12.5 Dầu khí
- Acid hóa giếng dầu
13. Tiêu chuẩn chất lượng HCl
HCl thương mại thường được phân loại:
| Loại | Nồng độ | Ứng dụng |
|---|---|---|
| HCl kỹ thuật | 30–32% | Công nghiệp |
| HCl tinh khiết | ≥35% | Phòng thí nghiệm |
| HCl thực phẩm | theo tiêu chuẩn | Thực phẩm |
14. An toàn trong sản xuất và sử dụng
HCl là hóa chất nguy hiểm, cần lưu ý:
- Trang bị bảo hộ: găng tay, kính, mặt nạ
- Tránh hít khí HCl
- Lưu trữ trong bồn nhựa hoặc composite
- Có hệ thống xử lý rò rỉ
15. Xu hướng công nghệ sản xuất HCl hiện đại
- Tự động hóa hệ thống
- Tháp hấp thụ hiệu suất cao
- Giảm phát thải khí
- Tái sử dụng nhiệt
- Tối ưu năng lượng
16. Kết luận
Phương pháp sản xuất HCl từ phản ứng giữa Hydro và Clo kết hợp hệ thống hấp thụ là công nghệ tiêu chuẩn trong công nghiệp hóa chất. Quy trình này mang lại hiệu suất cao, chi phí thấp và dễ kiểm soát chất lượng sản phẩm.
Việc hiểu rõ cấu tạo hệ thống gồm tháp tổng hợp và các tháp hấp thụ giúp doanh nghiệp:
- Tối ưu sản xuất
- Giảm chi phí vận hành
- Đảm bảo an toàn và môi trường
17. Liên hệ tư vấn và cung cấp HCl
Nếu bạn cần tư vấn kỹ thuật, báo giá hoặc cung cấp Axit Clohydric (HCl) 32% – 35%, hãy liên hệ:
CÔNG TY TNHH HÓA CHẤT THUẬN NAM
📍 Địa chỉ: 1/11D, Tổ 8B, KP3, Trảng Dài, Biên Hòa, Đồng Nai
📞 Hotline/Zalo: 0938 414 118
📧 Email: thunaco@gmail.com
🌐 Website: https://hoachatthuannam.com
Chúng tôi cung cấp HCl chất lượng ổn định, giá cạnh tranh, hỗ trợ kỹ thuật tận nơi cho doanh nghiệp sản xuất.